PI: Dott. Mario Capasso
Ricercatore in Genetica Medica – Università degli Studi di Napoli Federico II
PI: Prof. Achille Iolascon
Prof. Ordinario di Genetica Medica – Università degli Studi di Napoli Federico II
Durata del progetto: 3 anni
Costo del progetto: 249,000 euro
Razionale
Il neuroblastoma (NB) è un tumore pediatrico che rappresenta il 15% di morbilità e mortalità infantile per cancro. Il NB è caratterizzato da una notevole variabilità fenotipica e presenta decorsi clinici ampiamente divergenti. Recentemente si sta cercando di sviluppare terapie con lo scopo di trattare specifici pazienti con un NB ad alto rischio. Queste terapie includono l’utilizzo di farmaci inibitori del dominio chinasico del recettore del linfoma anaplastico (ALK) e dell’anticorpo monoclonale ch14.18 diretto contro il disialoganglioside GD2 specifico delle cellule tumorali. L’applicazione di terapie mirate per i pazienti ad alto rischio ha determinato un notevole aumento della sopravvivenza del 46-66%. Tuttavia, nonostante questi recenti progressi circa il 60% dei pazienti con tumori ad alto rischio muoiono a causa della ricaduta, cioè della ricomparsa della malattia dopo il trattamento.
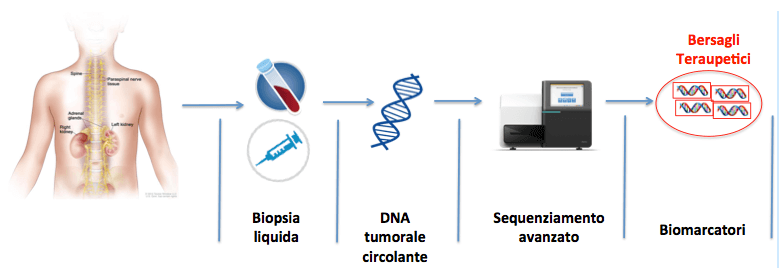
Recenti lavori hanno riportato che il numero di mutazioni del DNA di un tumore alla recidiva o delle metastasi è notevolmente superiore a quello rilevato nel tumore primario. Queste mutazioni presenti nelle metastasi e nella recidiva comportano il fallimento delle attuali terapie per la cura di questa devastante malattia. Quindi la comprensione dell’evoluzione delle mutazioni tumorali, dal primario alla metastasi e la progressione tumorale dall’esordio alla recidiva, ci consentirà di fornire delle terapie mirate ad eradicare i cloni cellulari più resistenti per diminuire o eliminare il rischio di ricaduta. Tutto ciò po’ essere ancora di più facilmente traslabile nella clinica perché ora è possibile isolare il DNA del tumore direttamente dal sangue periferico (DNA tumorale circolante) del paziente senza nessun intervento chirurgico. Questa metodica non invasiva è detta “biopsia liquida”.
Scopo
Lo scopo del presente progetto è di
– scoprire le mutazioni del DNA del tumore metastatico e recidivato che possono essere trattate con farmaci di nuova generazione e che possono essere utilizzate come biomarcatori della progressione della malattia
– sviluppare un metodo di identificazioni di tali biomarcatori/mutazioni non-invasivo detto “biopsia liquida”
Disegno sperimentale
Scopo 1. L’identificazione di mutazioni bersagliabili con farmaci offrirà la possibilità di progettare una terapia mirata per i tumori più aggressivi per evitare la recidiva e terapie personalizzate per pazienti che sviluppano la recidiva. A tal fine proponiamo per ciascun paziente il sequenziamento di tutto il genoma di cellule tumorali raccolte a due momenti diversi: all’esordio (tumore primario e metastasi al midollo) e alla recidiva (midollo). L’identificazione di mutazioni bersagliabili che si riscontrano all’esordio nelle cellule disseminate al midollo e non nel tumore primario ci darà indicazione dei cloni che si sono selezionati nella formazione di foci secondari e quindi responsabili della aggressività tumorale. Una terapia mirata ai specifici cloni metastatici consentirà un trattamento più efficace. In un secondo momento, l’analisi del genoma del tumore alla recidiva ci indicherà le mutazioni acquisite in seguito al trattamento che hanno reso il tumore resistente alla terapia. Queste informazioni consentiranno di disporre di una terapia personalizzata efficace e precisa.
Scopo 2. La lista di mutazioni generata dal sequenziamento dei tumori all’esordio e alla recidiva (Scopo 1) ci fornirà oltre a bersagli farmacologici anche nuovi biomarcatori prognostici che potranno essere utilizzati per decidere il percorso terapeutico del paziente e per verificare in corso di trattamento se la terapia sta funzionando. Il metodo meno invasivo per condurre il proposto percorso clinico diagnostico sarà collezionare biopsie liquide dei paziente a partire da un prelievo di sangue periferico al momento della diagnosi, durante trattamento e al follow-up. In seguito il sequenziamento del DNA tumorale circolante rilevato nel sangue periferico avrà potere predittivo sulla risposta terapeutica.
Prospettive future. Il completamento del progetto porterà all’identificazione di nuove mutazioni associate ad aggressività e resistenza nel NB ad alto rischio. I nostri risultati avranno un forte impatto in clinica nel predire la risposta alla terapia e nel realizzare una medicina personalizzata al fine di aumentare la sopravvivenza in questo sotto-gruppo di pazienti. Inoltre il completamento del progetto porterà alla valutazione di nuove strategie terapeutiche già in fase pre-trattamento. Infatti l’analisi del DNA tumorale circolante all’esordio della malattia sarà una metodica non-invasiva con un forte valore prognostico predittivo, un aspetto molto importante nei tumori pediatrici.
Metodi
Scopo 1. Per monitorare l’evoluzione della malattia e la resistenza alla terapia il tumore primario e metastasi al midollo osseo dallo stesso paziente saranno raccolti al momento della diagnosi e dopo la terapia (cicli ad alta intensità di dose di chemioterapia). L’analisi del sequenziamento del genoma (WGS) delle cellule tumorali sarà confrontata con l’analisi del sequenziamento del genoma del DNA costituzionale per identificare le mutazioni somatiche accorse nel tessuto tumorale. Come studio pilota, la raccolta di campioni da 15 pazienti sarebbe adatta per fornire informazioni molecolari significative a livello statistico come precedentemente pubblicato (7, 8). Sarà effettuato un WGS con una copertura di 60x (Illumina Hiseq 1500). In seguito, un sequenziamento con copertura maggiore (Deep-sequencing, copertura: 500x) sarà effettuato per validare le mutazioni rilevate nel WGS. L’analisi bioinformatica dei dati consentirà di rilevare varianti a singolo nucleotide e variazioni strutturali dei cromosomi.
Scopo 2. DNA tumorale circolante sarà estratto da sangue periferico prelevato da pazienti affetti da NB ad alto rischio. I campioni saranno prelevati a momento dell’esordio, durante il trattamento e al follow-up. WGS sarà eseguito su tali campioni tumorali come descritto sopra. L’insieme delle mutazioni identificate e validate in Scopo 1, saranno valutate su campioni di DNA tumorale circolante mediante metodiche di sequenziamento ad alta copertura genomica (Deep-sequencing).
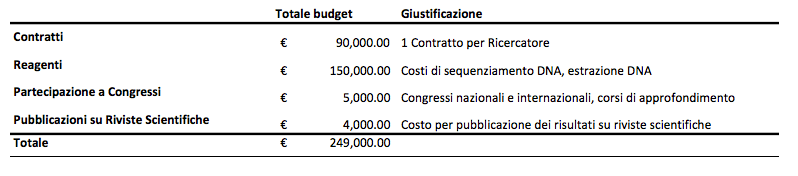
Suddivisione dei Costi

Via Andrea Laurogrotto, 19
84135 Salerno
Presso Ospedale Pausilipon
Via Posillipo, 226 – 80121 Napoli
Codice Fiscale
95086500659